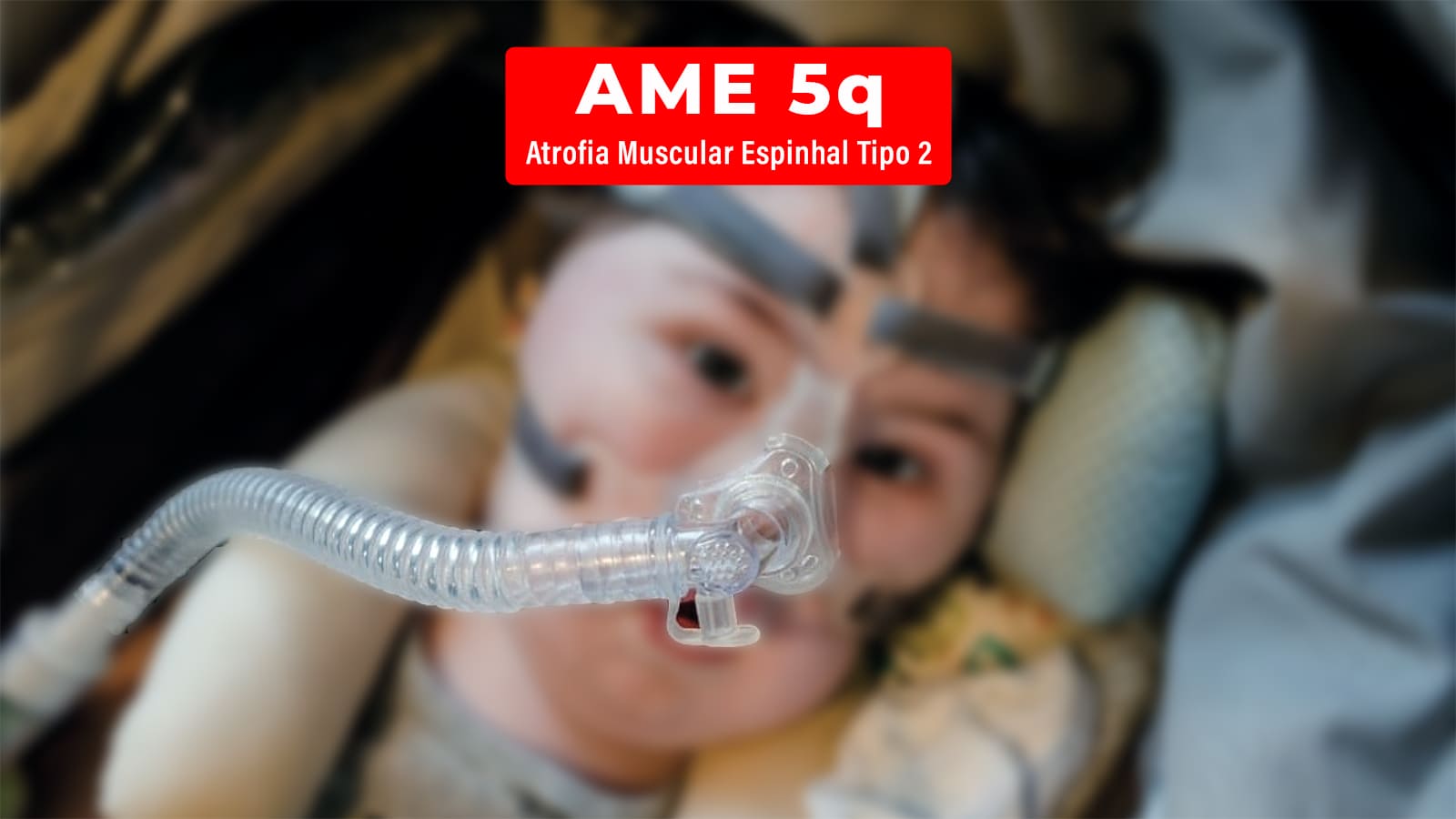
Após consulta pública com mais de 500 contribuições da sociedade civil, Ministério da Saúde atualiza Protocolo para tratamento da AME no SUS
A Biogen Brasil Produtos Farmacêuticos Ltda. (Biogen), empresa de biotecnologia com foco em neurociência, informa que o Ministério da Saúde, por meio da Secretaria de Ciência, Tecnologia, Inovação e Insumos Estratégicos em Saúde (SCTIE), atualizou o Protocolo Clínico e Diretrizes Terapêuticas (PCDT) para atrofia muscular espinhal (AME) 5q. A decisão foi oficializada no Diário Oficial da União (DOU) em 31 de janeiro .
Com a atualização, o documento que visa garantir o melhor cuidado à saúde, agora estabelece que “serão elegíveis ao tratamento, com o nusinersena, pacientes com AME tipo II com início dos sintomas entre 6 e 18 meses de vida, que tenham 12 anos de idade no início do tratamento ou mais de 12 anos de idade no início do tratamento com capacidade de sentar-se sem apoio e a função de membros superiores preservadas.”
O processo de atualização do PCDT foi iniciado no ano passado. A recomendação preliminar da Conitec, que foi levada à consulta pública Nº 81 , apresentava restrições ao tratamento. De acordo com o texto, seriam elegíveis apenas pacientes com AME tipo II com até 12 anos de idade. Escoliose grave e/ou contratura grave também eram considerados critérios de exclusão. Contudo, essas recomendações iniciais foram revertidas.
“A atualização do PCDT é uma vitória importante para quem convive com uma doença neurodegenerativa e não pode deixar de se tratar. Com essa decisão do Ministério da Saúde, um perfil mais amplo de pacientes com AME tipo II será beneficiado com o tratamento pela rede de saúde pública”, explica Tatiana Rivas Marante, gerente geral da Biogen Brasil.
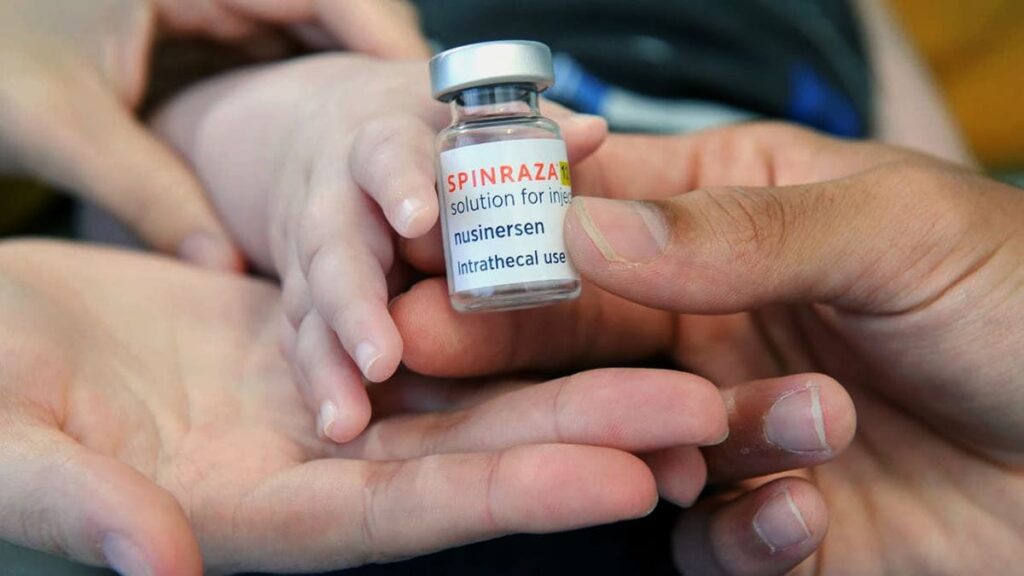
De acordo com a publicação do DOU, a portaria Nº 03 já está em vigor. Atualmente, mais de 11 mil pacientes já fazem uso do nusinersena no mundo, 57 países garantem algum tipo de acesso ao medicamento. Dentre esses, 40 já trabalham com processos formais de acesso dentro de seus territórios. No Brasil, o tratamento foi o primeiro aprovado pela Agência Nacional de Vigilância Sanitária (Anvisa) para AME 5q sem distinção de subtipos, peso, idade ou condição clínica .
Saiba mais sobre a atrofia muscular espinhal
A AME é uma das mais de 8 mil doenças raras conhecidas no mundo e afeta, aproximadamente, entre 7 a 10 bebês em cada 100 mil nascidos vivos, sendo a maior causa genética de morte em crianças de até dois anos de idade. Se caracteriza por uma fraqueza progressiva, que compromete funções como respirar, comer e andar. No Brasil, ainda não há um estudo epidemiológico que indique o número exato de indivíduos afetados pela doença. A doença é classificada clinicamente em tipos (que vão do tipo 0 ao 4), com base no início dos sinais e sintomas e nos marcos motores atingidos pelos pacientes.
SOBRE A BIOGEN
Como pioneira em neurociência, a Biogen descobre, desenvolve e oferece terapias inovadoras em todo o mundo para pessoas que vivem com doenças neurológicas graves, bem como adjacências terapêuticas relacionadas. Uma das primeiras empresas globais de biotecnologia do mundo, a Biogen foi fundada em 1978 por Charles Weissmann, Heinz Schaller, Sir Kenneth Murray e os vencedores do Prêmio Nobel Walter Gilbert e Phillip Sharp. Hoje, a Biogen tem o portfólio líder de medicamentos para tratar a esclerose múltipla e introduziu o primeiro tratamento aprovado para atrofia muscular espinhal.
A Biogen também está se concentrando no avanço do pipeline mais diversificado da indústria em neurociência, que transformará o padrão de atendimento para pacientes em várias áreas de grande necessidade não atendida.
Em 2020, a Biogen lançou uma iniciativa ousada de 20 anos e US$250 milhões para abordar as questões profundamente inter-relacionadas de clima, saúde e equidade. Healthy Climate, Healthy Lives™ tem como objetivo eliminar os combustíveis fósseis em todas as operações da empresa, construir colaborações com instituições renomadas para o avanço da ciência para melhorar os resultados de saúde humana e apoiar comunidades carentes.
Continuamente, a empresa divulga informações em seu site que podem ser importantes aos investidores.
LINKS ÚTEIS:
- Website: https://www.biogen.com/
- Twitter: https://twitter.com/biogen/
- LinkedIn: https://www.linkedin.com/company/biogen-/
- Facebook: https://www.facebook.com/Biogen/
- YouTube: https://www.youtube.com/biogen/